Τα μυστικά της φωτιάς
Εκ πρώτης όψεως φαντάζει μια ερώτηση που μονάχα ένα παιδί θα έκανε. Όμως όσο περισσότερο την σκεφτόμαστε, τόσο περισσότερο καταλαβαίνουμε ότι ίσως και να μην γνωρίζουμε την απάντηση όσο καλά θεωρούμε.
Η φωτιά υπάρχει στη διάθεση του ανθρώπου από αρχαιοτάτων χρόνων. Βοήθησε τους προγόνους μας να επιβιώσουν τις τότε καιρικές συνθήκες και τους έδωσε εύκολη πρόσβαση σε τροφή και προστασία από τους θηρευτές. Η απάντηση στην φύση και τη λειτουργία αυτής της μυστήριας ουσίας κρύβεται σε αυτό που σήμερα ονομάζουμε επιστήμη της Χημείας.
Η διαδικασία της παραγωγής φλόγας
Η φωτιά δεν είναι τίποτα άλλο από μια αλληλουχία χημικών αντιδράσεων. Κατά βάση αυτό που βλέπουμε όταν ανάβουμε ένα σπίρτο είναι συνεχόμενες χημικές αλληλεπιδράσεις όπου τα παραγόμενα προϊόντα τους είναι : θερμότητα, φως και αέρια. Στην κόκκινη κορυφή του σπίρτου για παράδειγμα εντοπίζονται 2 χημικά στοιχεία που είναι υπεύθυνα για την παραγωγή φλόγας, το Θείο και ο κόκκινος Φώσφορος. Από τη σπίθα που προκαλείται λόγω της τριβής τα 2 αυτά στοιχεί αναφλέγονται.
Εικόνα 1. Η ανάφλεξη ενός τυπικού σπίρτου.
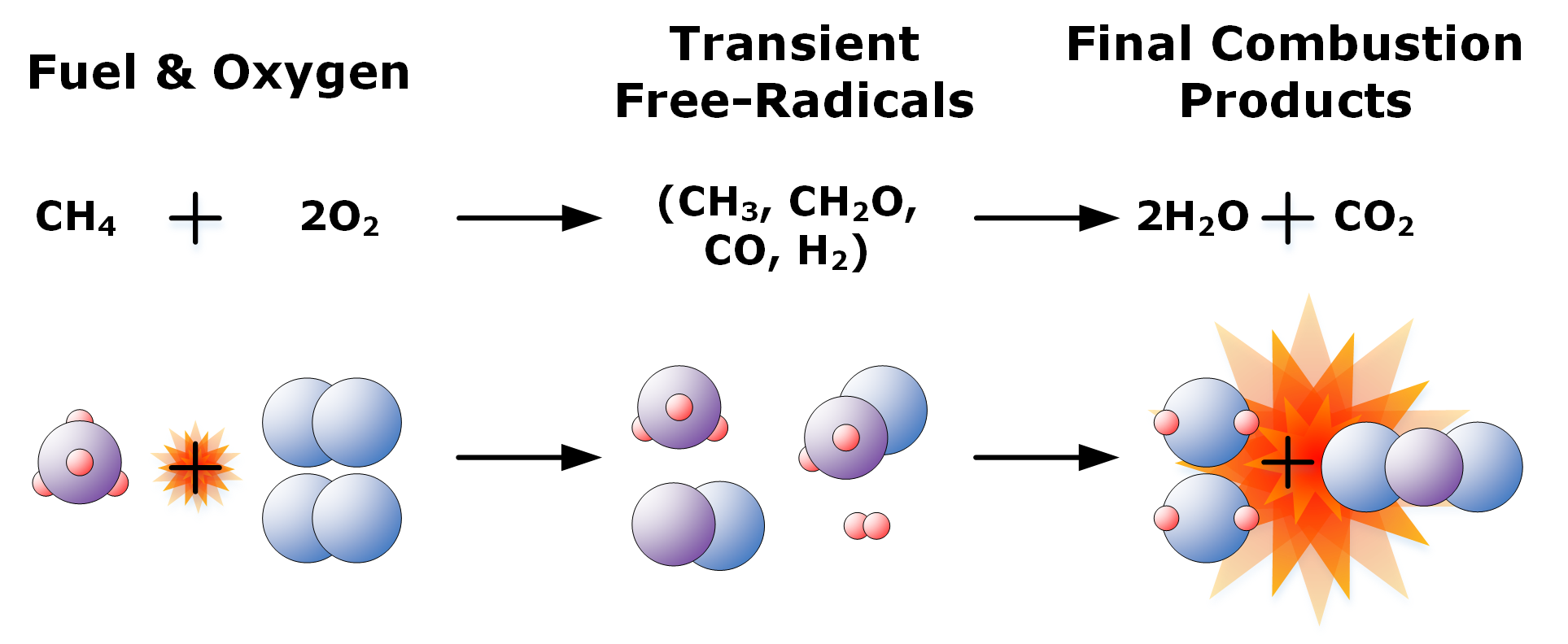
Επομένως για να παράξουμε φωτιά χρειαζόμαστε μονάχα 3 συστατικά: οξυγόνο, μια πηγή καυσίμου και θερμότητα. Ενώ το οξυγόνο και η θερμότητα είναι απαραίτητα στοιχεία η πηγή καυσίμου μπορεί να είναι το οτιδήποτε. Τα δυο πιο εύφλεκτα στοιχεί στη Γη είναι το υδρογόνο και ο άνθρακας, συνεπώς τα καύσιμα με τη μεγαλύτερη περιεκτικότητα σε αυτά τα στοιχεία είναι και οι ιδανικοί υποψήφιοι. Με την απελευθέρωση μια αρχικής θερμικής ενέργειας π.χ μιας σπίθας από ένα σπίρτο το εκάστοτε καύσιμο πρέπει να φτάσει στην δική του ξεχωριστή θερμοκρασία ανάφλεξης. Μόλις ζεσταθούν τα καύσιμα απελευθερώνουν πτητικά αέρια και ξεκινούν τις αλυσιδωτές αντιδράσεις οξείδωσης που αποκαλούμε καύση. Κατά τη διάρκεια της οξείδωσης οι χημικοί δεσμοί του καυσίμου σπάνε κι απελευθερώνονται τα προϊόντα της καύσης – διοξείδιο του άνθρακα και νερό. Τέλος κατά το σπάσιμο των δεσμών παρατηρούμε την απελευθέρωση ενέργειας σε μορφή θερμότητας και φωτός.
Αξίζει να αναφέρουμε σε αυτό το σημείο πως δεν διαθέτουν όλες οι φλόγες αυτό το χαρακτηριστικό κίτρινο – κοκκινωπό χρώμα που τις έχουμε συνηθίσει. Αντιθέτως η φωτιά μπορεί να έχει διάφορα χρώματα όπως πράσινο κίτρινο ή ακόμα και μοβ. Ο λόγος για αυτό το φαινόμενο ( αν και δε εμβαθύνουμε πολύ σε αυτό) είναι η κβαντομηχανική. Όταν δίνουμε ενέργεια (σε αυτή τη περίπτωση θερμική) σε ηλεκτρόνια αυτά μεταπηδούν από μια κατάσταση ηρεμίας σε μια διεγερμένη κατάσταση. Μπορούμε να φανταστούμε τα ηλεκτρόνια στη διεγερμένη κατάσταση σαν να έχουν περισσότερη ενέργεια εκείνη τη στιγμή. Μερικά από αυτά τα ηλεκτρόνια θα επιστρέψουν πίσω στην κανονική τους κατάσταση. Κατά τη επιστροφή τους εκπέμπουν ενέργεια σε μορφή κυμάτων διαφόρου μήκους, άρα και χρωμάτων.
Εικόνα 3. Απεικόνιση των διαφορετικών χρωμάτων της φωτιάς αναλογικά με το χημικό στοιχείο.
Αντιμετώπιση των πυρκαγιών – χρήση πυροσβεστήρων.
Ο πιο κοινός τρόπος αντιμετώπισης μιας ανεπιθύμητης φωτιάς μέχρι και σήμερα είναι οι πυροσβεστήρες. Πλέον εντοπίζονται παντού, σε σπίτια, σε μαγαζιά, ακόμα κι σε αυτοκίνητα. Σβήνουν όμως πραγματικά τις φωτιές ;
Αναφέραμε προηγουμένως ότι για να υπάρξει φωτιά χρειάζονται 3 συστατικά: θερμότητα, οξυγόνο και καύσιμο. Αν αφαιρέσεις ένα απο αυτά, η φωτιά θα σβήσει. Στο εσωτερικό του πυροσβεστήρα υπάρχουν 2 κύρια υλικά:
- Το κατασβεστικό υλικό. Μπορεί να είναι νερό, σκόνη και διοξείδιο του άνθρακα
- Το προωθητικό αέριο. Ένα αέριο υπό υψηλή πίεση (συνήθως άζωτο ή διοξείδιο του άνθρακα) που “σπρώχνει” το υλικό έξω με δύναμη.
Όταν τραβάμε την περόνη και πιέζουμε τη λαβή του πυροσβεστήρα συμβαίνουν τα εξής:
Απελευθερώνεται η πίεση επιτρέποντας στο προωθητικό αέριο να εκτονωθεί. Με τη σειρά του το αέριο πιέζει το κατασβεστικό υλικό προς τα κάτω. Επειδή δεν έχει πού αλλού να πάει, το υλικό ανεβαίνει μέσω ενός εσωτερικού σωλήνα προς το ακροφύσιο.
 Εικόνα 4. Διάγραμμα ενός τυπικού πυροσβεστήρα.
Εικόνα 4. Διάγραμμα ενός τυπικού πυροσβεστήρα.



