
Πολιτισμός



Ghost towns: από την εγκατάλειψη στον τουρισμό
Οι ghost towns ή αλλιώς πόλεις-φαντάσματα, έχουν γίνει σε όλο τον κόσμο τουριστικά αξιοθέατα. Η επίσκεψη σε ένα…
Κινηματογράφος

John Cazale: Ένα αστέρι που έσβησε νωρίς
Ο John Cazale θεωρείται πως είναι από τους πιο σημαντικούς ηθοποιούς που πέρασαν από το Hollywood και παρά την σύντομη καριέρα που είχε, άφησε το στίγμα…

Φεστιβάλ “ΑΓΩΝ” 2026!

Videodrome: Προφητικός και βίαιος τρόμος

Το νου σας, κατέφτασε η Νύφη!

Το CinePi Short Film Festival επιστρέφει!
Θέατρο

Κολακεία: Από τον Αισχύλο έως την Παπαδοπούλου
Εισαγωγή Η κολακεία αποτελεί ένα διαχρονικό φαινόμενο της ανθρώπινης συμπεριφοράς, στενά συνδεδεμένο με την εξουσία, την επιθυμία και την κοινωνική…




Βιβλίο

Όχι εγώ: ο Μπέκετ και το τραύμα της γλώσσας
Ας αρχίσουμε μ’ ένα λογοπαίγνιο. Το τραύμα της γλώσσας είναι δίλημμα: τραύμα…

Ποιοι τελικά διδάσκουν τη φιλαναγνωσία ;
Το βιβλίο δεν είναι μόνο αγάπη. Είναι πάθος. Είναι εμμονή. Είναι τρόπος ζωής!…

H ώρα είναι 12 παρά 12
Μπορεί να έχουμε Μάιο μήνα, όμως πολλοί από μας νοσταλγούμε το Χειμώνα…

“Λαμπερό Δέρμα Σε Κάθε Ηλικία” για όλες τις Γυναίκες
Δεν έχει πολύ καιρό που κυκλοφόρησε, από τις εκδόσεις Διάνοια, το…

Ο Νεκρός του Bataille ή Η ηδονή του θανάτου
Στη ψυχανάλυση, κι όχι μόνο, τα ένστικτα του έρωτα και του θανάτου…

Κρυμμένες Ζωγραφιές του Jason Rekulak
Το μυθιστόρημα Κρυμμένες Ζωγραφιές του Jason Rekulak κυκλοφόρησε από τις εκδόσεις Μεταίχμιο…
Μουσική

Gemma: “Μέσα από την μουσική μπορούμε να βγούμε από τον λαβύρινθο της πραγματικότητας”
Οι Gemma είναι ένα πενταμελές συγκρότημα που δημιουργήθηκε το 2017 στο Ρέθυμνο Κρήτης. Αποτελείτε από…

Κατερίνα Σμαραγδά: «Ευτυχώς εγώ έχω εσένα»
Πόσες φορές δεν έχουμε πει στην ζωή μας «Ευτυχώς εγώ έχω εσένα»; Αυτό μας λέει…
Ταξίδια

Tύμπινγκεν: Μια ανοιξιάτικη έκπληξη στη Γερμανία
Tύμπινγκεν Πηγή: newsbeast.gr Το Tύμπινγκεν είναι μία μικρή πόλη της Σουαβίας στο κρατίδιο της Βάδης-Βυρτεμβέργης στη νότια Γερμανία και η αλήθεια είναι, δεν σου έρχεται εύκολα…
Ψυχολογία

Όταν η ταυτότητα αλλάζει: οι μικρές μεταμορφώσεις της ζωής
https://images.unsplash.com/ Υπάρχουν στιγμές στη ζωή που δεν μοιάζουν με τεράστιες αλλαγές. Δεν είναι δραματικές και ούτε συνοδεύονται από θόρυβο. Αντιθέτως,…

Η ψυχολογία του «ανήκειν»


Η ψυχολογία της ανασφάλειας

Μόδα

Dior vs Chanel: Τα φαντάσματα πίσω από τους δύο θρύλους
Αφιέρωμα στο «The New Look» κάνει ο Codd Kessler με την νέα…

Τα πιο stylish και cozy looks για τα χιόνια
Ο καιρός έχει αρχίσει σιγά σιγά επιτέλους να κρυώνει. Σε πολλές περιοχές,…

Γκαρνταρόμπα: Τρόποι οργάνωσης για να φτιάχνεις εύκολα fashionable looks
Πόσες είναι οι φορές που δε βρίσκουμε τίποτα να φορέσουμε και μας…

Με αυτά τα outfits θα εντυπωσιάσεις εάν είσαι καλεσμένη σε γάμο
Καθώς μπήκε η wedding season, η αναζήτηση του τέλειου outfit είναι γεγονός.…

Τα πιο stylish πέδιλα για να φτιάξεις τα καλοκαιρινά looks
Είτε high είτε mid, τα πέδιλα θα είναι πάντα η λατρεία των…

Τα αγαπημένα μας καλοκαιρινά looks με τα λινά ρούχα
Ανέκαθεν, τα λινά ρούχα θεωρούνταν “βασιλικά” υφάσματα, καθώς προορίζονταν κυρίως για τις…
Τεχνολογία & Επιστήμη

Ο ανθώπινος νους ως σύστημα διαχείρισης έργων.
Μήπως τελικά είμαστε όλοι “project managers”; Έχεις παρατηρήσει ότι η μέρα σου μοιάζει με μια…

Ενάμιση Χιλιόμετρο Κάτω από τη Γη, στο Κυνήγι του Αόρατου Σύμπαντος
Ενάμιση Χιλιόμετρο Κάτω από τη Γη, στο Κυνήγι του Αόρατου Σύμπαντος Ο Γαλαξίας πάνω από…
Αψυχολόγητα

Love language: Η γλώσσα της αγάπης σου είναι η δύναμη σου
Δεν αγαπάμε όλοι με τον ίδιο τρόπο — και αυτό δεν είναι καθόλου πρόβλημα. Αντιθέτως είναι δύναμη. Η γλώσσα αγάπης που κουβαλάει ο καθένας μας, δεν…

Οι Τρίτες μου δεν είναι πια ίδιες

Μεταξύ «ιδανικών»

Δεν φοβόμαστε την αγάπη, αλλά το κόστος της

Κάθε πόνος είναι πέρασμα
Συνεντεύξεις
Πρόσωπα, δημιουργοί και ιστορίες μέσα από τις πιο ενδιαφέρουσες συζητήσεις του MAXMAG.
“Η ψυχική υγεία ως γέφυρα για μια καλύτερη ζωή”: Συνέντευξη με την Ιωάννα Αλπέρτη
Θερμές ευχαριστίες στην κα Ιωάννα Αλπέρτη, Επιστημονικά Υπεύθυνη του Iasis at Centro, για την εμπεριστατωμένη συνέντευξή της. Μέσα από τις δράσεις της και τη δέσμευσή της στον τομέα…

Μαρια Λεντζου: Η ομορφιά του να είσαι γυναίκα μέσω της Αυθεντικής Κίνησης
Τι σημαίνει άραγε «να είμαστε εντάξει με τον εαυτό μας» ως γυναίκες; Και πως μπορούμε -η κάθε…

Νίκος Μαντάς: «Δεν μπορώ να φανταστώ έναν έρωτα να μοιράζεται»
Ο Νίκος Μαντάς με τη γραφή του εκπλήσσει, προβάλλει το νόημα, το σημαντικό. Είναι ο σημερινός καλεσμένος…

Κλειώ Ιερωνυμάκη: «Έγραφα από μικρό παιδί»
Η Κλειώ Ιερωνυμάκη είναι μαζί στη στήλη των συνεντεύξεων για μια συζήτηση για το βιβλίο της “Ο…

Σοφία Ιωσηφίδου: Στην Κορυφή των Εμποδίων στην Ελλάδα
Βρίσκεται ανάμεσα στις καλύτερες αθλήτριες στα 60 και 100 μέτρα με εμπόδια στην Ελλάδα. Η Σοφία Ιωσηφίδου,…
Αφιερώματα
Μεγάλα θέματα, πρόσωπα και ιστορίες που αξίζουν περισσότερο χώρο και βαθύτερη ανάγνωση.
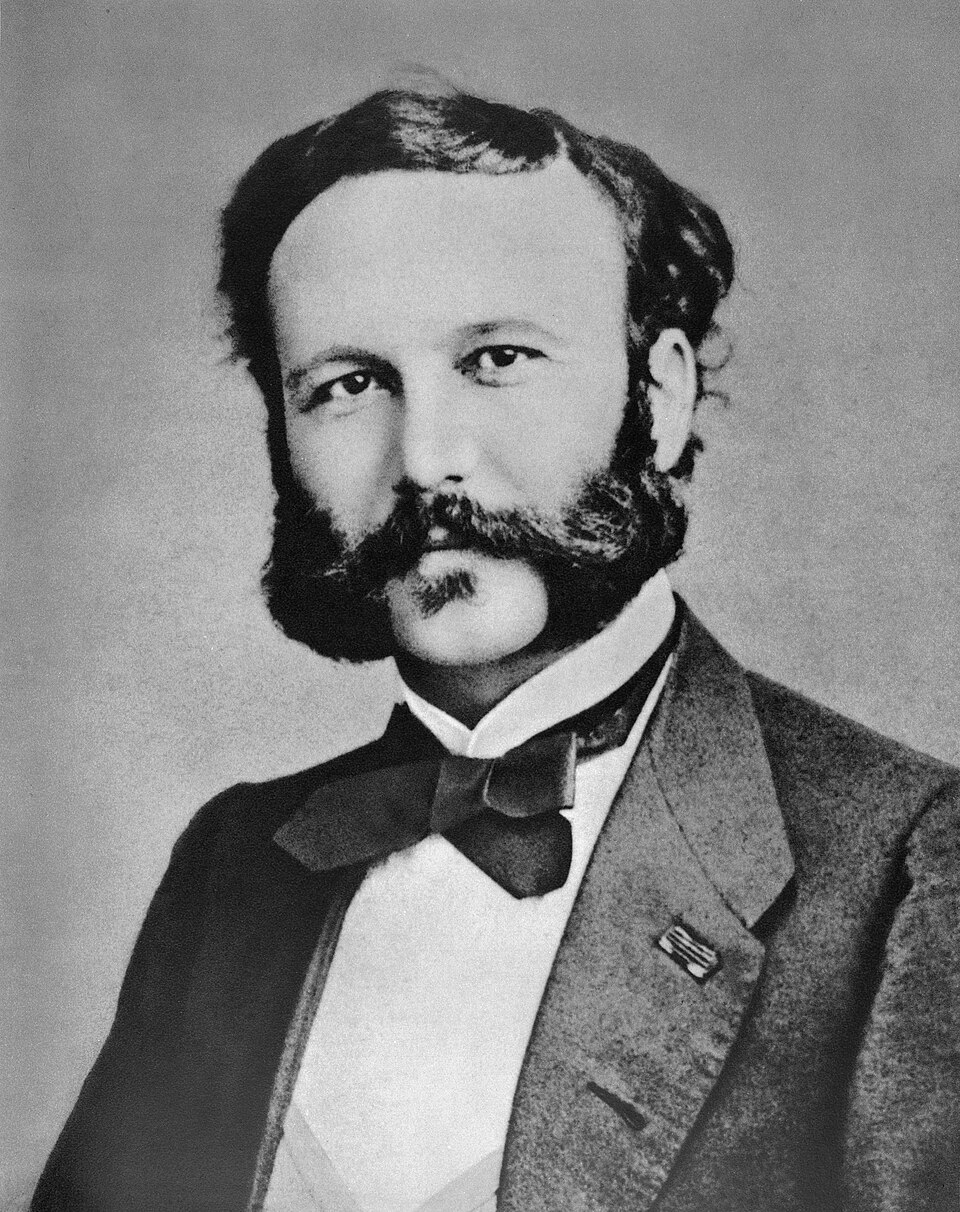 Αφιερώματα
Αφιερώματα
Ερρίκος Ντυνάν: Ο ιδρυτής του Ερυθρού Σταυρού
Ο Ερρίκος Ντυνάν (Jean Henri Dunant) ήταν ιδρυτής του Ερυθρού Σταυρού και ο πρώτος που…
 Αφιερώματα
Αφιερώματα
Η κυκλοφορία του Pac-Man το 1980
Το 1980 αποτέλεσε μια χρονιά-σταθμό για τη βιομηχανία των βιντεοπαιχνιδιών, καθώς τότε κυκλοφόρησε το θρυλικό…
4 Ιουνίου 1961: Η κρίση του Βερολίνου
Στις 4 Ιουνίου 1961, η παγκόσμια πολιτική σκηνή βρέθηκε σε ένα από τα πιο τεταμένα της σημεία κατά τη διάρκεια…
 Αφιερώματα
Αφιερώματα
Ευλογιά: Η εξάλειψη μιας θανατηφόρας επιδημίας
Η ευλογιά ήταν μολυσματική ασθένεια που προσέβαλλε αποκλειστικά τον άνθρωπο και την προκαλούσαν δύο στελέχη…
 Αφιερώματα
Αφιερώματα
16 Μαΐου 1929: Η πρώτη τελετή των Όσκαρ
Στις 16 Μαΐου 1929 πραγματοποιήθηκε στο Hollywood Roosevelt Hotel η πρώτη απονομή των βραβείων Όσκαρ,…
Άγνωστη Ελλάδα
Κρυφές διαδρομές, χωριά και ελληνικά μέρη έξω από τους συνηθισμένους χάρτες.
City Guide
Η πόλη σε πρώτο πλάνο: στέκια, έξοδοι, διαδρομές και μικρές διευθύνσεις που αξίζει να ανακαλύψεις.































